医疗器械生产经营企业(GMP、GSP)质量管理体系规范 高级研修项目
时间:2019年8月12-14日
地点:上海市长江路43号
主办:上海理工大学国家级专业技术人员继续教育基地;上海理工大学医疗器械与食品学院、上海介入医疗器械工程技术研究中心
支持:中城Comp@ss、绿字(上海)信息科技有限公司(ITTN上海中心)、北京国医械华光认证有限公司
研修内容:
(一)理论授课部分:
1、医疗器械法规(适用于所有医疗器械从业人员)
《医疗器械监督管理条例》国务院令第680号
《医疗器械生产质量管理规范》重点条款解读
企业容易出现的问题与应对措施
2、管理者代表(适用于医疗器械生产经营企业负责人、管理者代表、质量人员)
管理者代表的职责、权限和能力要求
如何制定和实施质量方针和质量目标
如何建立融入法规要求的体系文件
如何将法规与风险管理融入质量管理体系
如何做好内审活动
如何提高管理评审的效果
介绍质量成本管理、5S管理和卓越绩效等企业现代 管理模式
专题研讨:质量管理体系常见问题
(二)现场教学
医院、政府机构、企业现场参观交流。
研修亮点:
培训学时计入专业技术人员继续教育学时;
擅长医疗器械组织管理者代表、ISO13485和ISO 9001内审员、医疗器械生产质量管理规范等专题培训;
了解中国及国际医疗器械最新政策、医疗器械热点方向;
与投资方、医疗器械产业的商界合作伙伴面对面交流;
相关活动宣讲会:上海介入医疗器械工程技术研究中心口腔科专业委员会成立仪式、第3届世界医疗器械设计(中国)大会暨中国国际医疗器械创新技术展览会、第四届中国创新挑战赛(上海)暨第二届长三角国际创新挑战赛国际智能医疗器械专场。
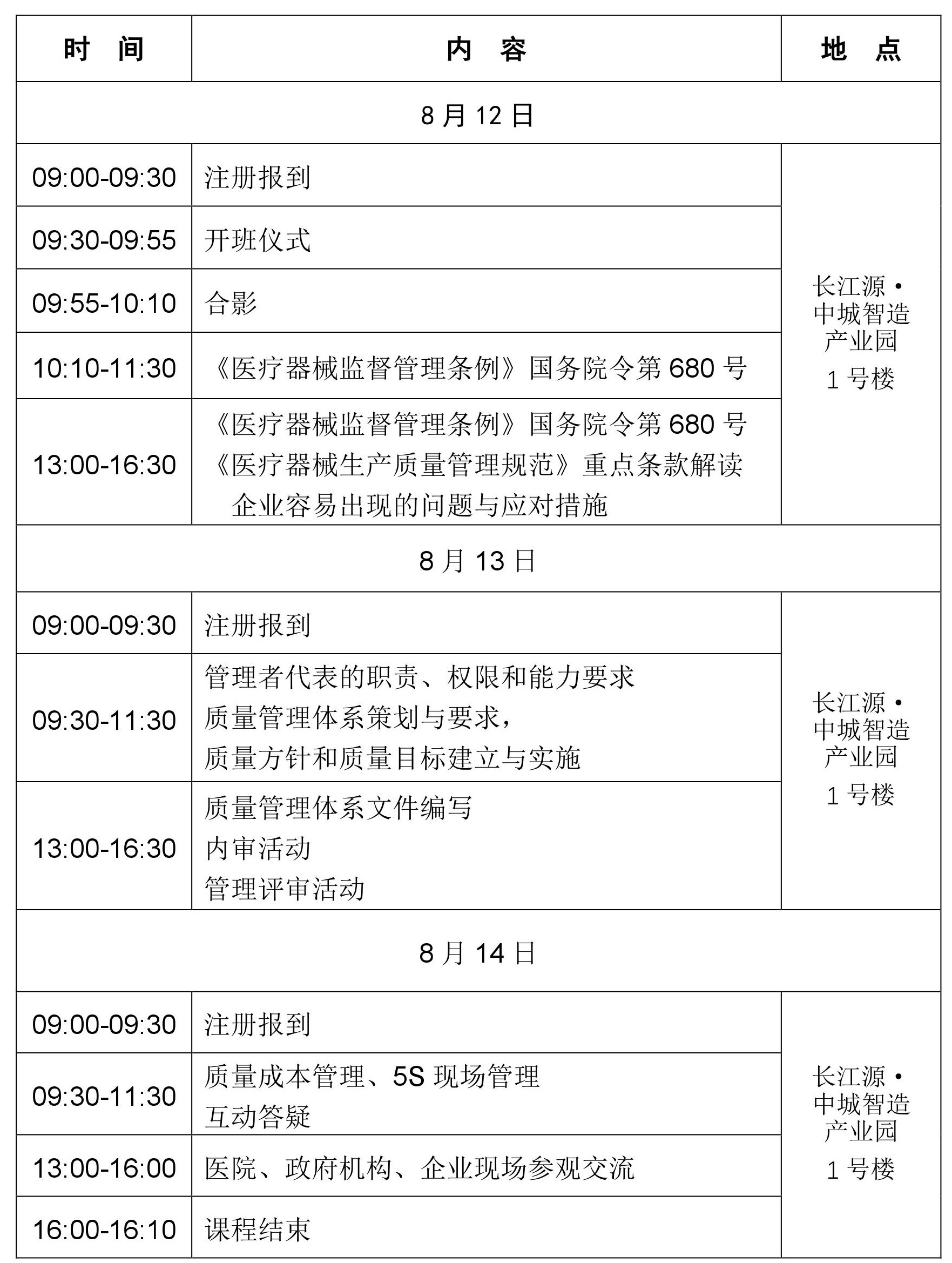
日程
研修对象:
医疗科技领域高级专业技术人员、高层管理人员,具体包括:生物医药、医疗器械生产制造商、政府监管机构、科研院所、医院、检验所等相关从业人员,预40人。
名额有限,最终录取名单将从报名人选中研究讨论决定,筛选符合条件的学生并发布通知。
其他事项:
(一)研修人员修完规定课程、经考核合格后,培训学时计入专业技术人员继续教育学时。学员凭姓名和身份证号注册并登录专业技术人才知识更新工程公共服务平台http://www.sacee.org.cn/,查询本人学时。
(二)按照文件规定,高级研修项目经费由上海市财政全额资助,包括伙食费、培训场地费、讲课费、培训资料费等,不向学员收取。往返交通费由学员自行承担。
(三)为进一步增强创新优势和产业优势相互转化能力,加深长三角区域创新要素互融互通、政策服务协同,加强与国际创新资源联动,2019年5月-12月将持续举办第四届中国创新挑战赛(上海)暨第二届长三角国际创新挑战赛。上海理工大学、中城生物医学工程Comp@ss作为本次大赛服务机构,特别设置“国际智能医疗器械专场”。欢迎提出需求,我们将为您在全球范围寻求解决方案。




